神經(jīng)干細胞與人體干細胞技術(shù) 開發(fā)現(xiàn)狀與應(yīng)用前景簡述
干細胞技術(shù)是現(xiàn)代生命科學和再生醫(yī)學的核心領(lǐng)域之一,其中神經(jīng)干細胞技術(shù)和更廣義的人體干細胞技術(shù)正引領(lǐng)著生物醫(yī)學研究的深刻變革。本報告旨在簡述這兩項技術(shù)的發(fā)展概況及其應(yīng)用潛力。
一、 技術(shù)概述
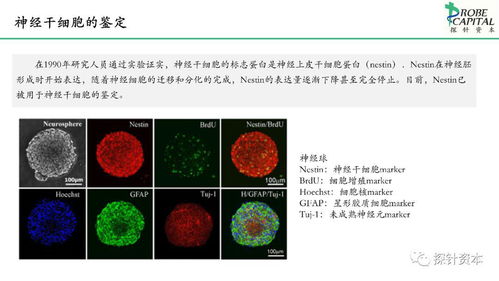
- 神經(jīng)干細胞技術(shù):神經(jīng)干細胞是指存在于中樞神經(jīng)系統(tǒng)(腦和脊髓)中,具有自我更新能力并能分化為神經(jīng)元、星形膠質(zhì)細胞和少突膠質(zhì)細胞等多類神經(jīng)細胞的原始細胞。其技術(shù)核心在于對這類細胞的分離、體外培養(yǎng)擴增、定向誘導分化以及安全有效的移植。獲取來源包括胚胎、胎兒組織以及通過誘導多能干細胞技術(shù)重編程獲得。
- 人體干細胞技術(shù):這是一個更廣泛的概念,涵蓋對各類人體來源干細胞的開發(fā)利用。主要包括:
- 胚胎干細胞:源自早期胚胎,具有分化為幾乎所有人體細胞類型的“全能性”。
- 成體干細胞:存在于成年個體的各種組織(如骨髓、脂肪、皮膚等)中,負責組織的更新與修復,如造血干細胞、間充質(zhì)干細胞。
- 誘導多能干細胞:通過將體細胞(如皮膚細胞)重編程而獲得,具有類似胚胎干細胞的多能性,避免了倫理爭議,是個性化醫(yī)療的重要工具。
二、 主要開發(fā)進展
- 來源與獲取:從依賴胚胎組織,發(fā)展到利用成體組織提取,再到通過iPSC技術(shù)“創(chuàng)造”干細胞,來源日益豐富且倫理障礙逐步減小。
- 培養(yǎng)與擴增:開發(fā)了更安全、無動物源性成分的培養(yǎng)體系,實現(xiàn)了干細胞在體外的大量、穩(wěn)定擴增。
- 定向分化:通過調(diào)控特定的生長因子和信號通路,已能較精確地將干細胞誘導為特定功能細胞,如多巴胺能神經(jīng)元、心肌細胞、胰島β細胞等。
- 基因編輯結(jié)合:CRISPR等基因編輯技術(shù)與干細胞技術(shù)結(jié)合,可用于修正干細胞中的致病基因,或構(gòu)建疾病模型,極大地推動了研究與治療開發(fā)。
三、 應(yīng)用領(lǐng)域與前景
- 疾病建模與藥物篩選:利用患者來源的iPSC分化為病變細胞(如運動神經(jīng)元、肝細胞),在培養(yǎng)皿中構(gòu)建“疾病模型”,用于研究發(fā)病機制和篩選新藥,尤其適用于神經(jīng)退行性疾病(如阿爾茨海默病、帕金森病)、遺傳病等。
- 細胞替代治療:這是最受期待的應(yīng)用方向。
- 神經(jīng)領(lǐng)域:將分化的神經(jīng)細胞或前體細胞移植到受損腦區(qū),以替代因中風、脊髓損傷、帕金森病等而丟失的神經(jīng)元或膠質(zhì)細胞,修復神經(jīng)功能。已有針對帕金森病、脊髓損傷的臨床研究開展。
- 其他領(lǐng)域:利用造血干細胞移植治療白血病等血液疾病已是成熟療法;利用間充質(zhì)干細胞治療移植物抗宿主病、骨關(guān)節(jié)疾病等;探索用分化的心肌細胞修復心臟、用胰島細胞治療糖尿病等。
- 組織工程與器官再造:以干細胞作為“種子細胞”,結(jié)合生物材料構(gòu)建三維組織結(jié)構(gòu),目標是再造可用于移植的復雜組織或器官,如皮膚、角膜、軟骨乃至微型肝組織。
- 基因治療載體:經(jīng)基因修飾的干細胞可作為長期、穩(wěn)定的體內(nèi)治療蛋白分泌源,或作為攜帶治療基因的載體。
四、 挑戰(zhàn)與展望
盡管前景廣闊,該領(lǐng)域仍面臨重大挑戰(zhàn):干細胞移植后的存活率、整合效率、長期安全性(如致瘤風險)、免疫排斥問題以及規(guī)模化生產(chǎn)的質(zhì)量控制等。倫理與法規(guī)監(jiān)管也需持續(xù)完善。
隨著基礎(chǔ)研究的深化和技術(shù)的不斷突破,神經(jīng)干細胞與人體干細胞技術(shù)有望從實驗室和臨床試驗,逐步走向更廣泛的臨床應(yīng)用,為實現(xiàn)個性化、精準化的再生醫(yī)學治療,攻克眾多難治性疾病帶來革命性的希望。技術(shù)的融合(如干細胞與生物材料、人工智能的結(jié)合)將進一步加速這一進程。
如若轉(zhuǎn)載,請注明出處:http://www.psoemu.cn/product/29.html
更新時間:2026-04-20 04:50:47